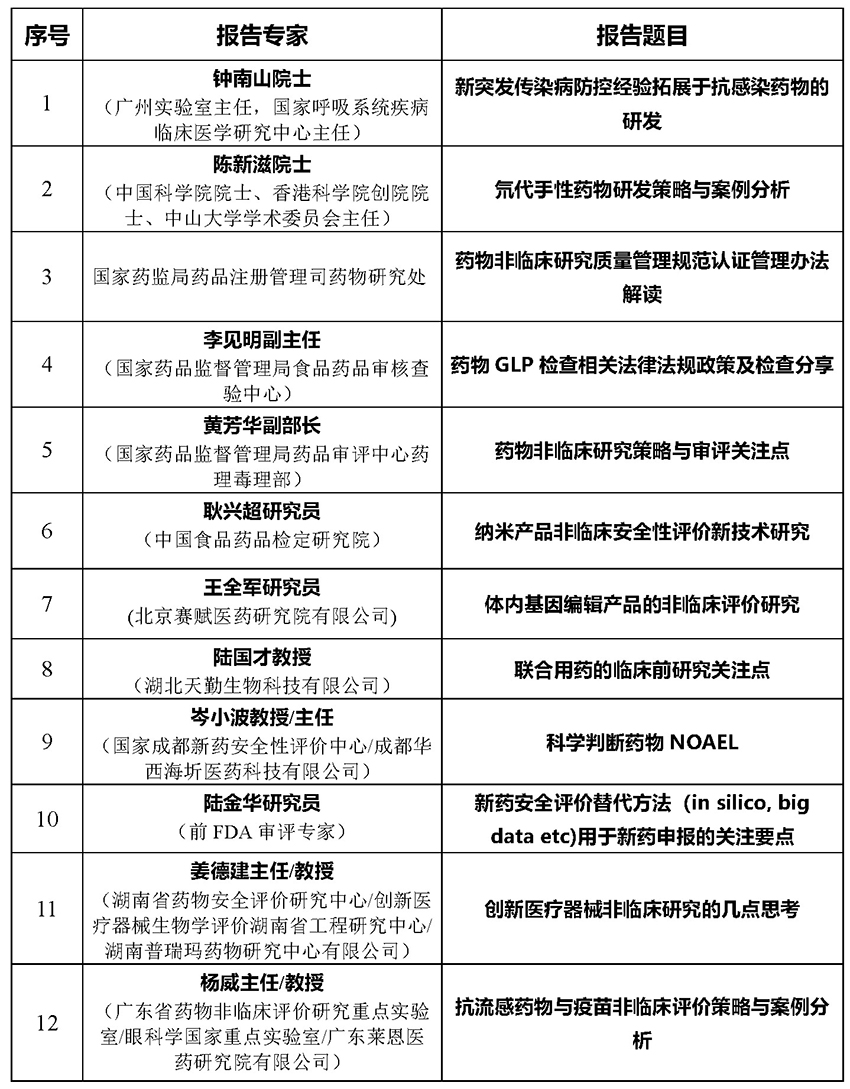
大会特邀报告,将邀请院士、我国和美国的药物审评专家、上市公司技术总裁和具有一线医药研发经验的专家。分论坛将根据“政策”、“学术”和“产业”三方面内容安排,邀请国内外富有学术和政策咨询方面经验的专家、学者和官员演讲。聚焦国内外创新药物研发与临床前安全性评价研究最新动态和国内外药物毒理学基础与应用研究最新进展;对接国际规范,把控ICH指导原则全面落地实施与未来发展规划;鼓励医药创新,促进产业发展。同时将召开国际创新医药研发企业学术交流与产品研发对接卫星会。
(以下为已邀请到的国内药物GLP检查专家;2023年6月17日08:30-12:10
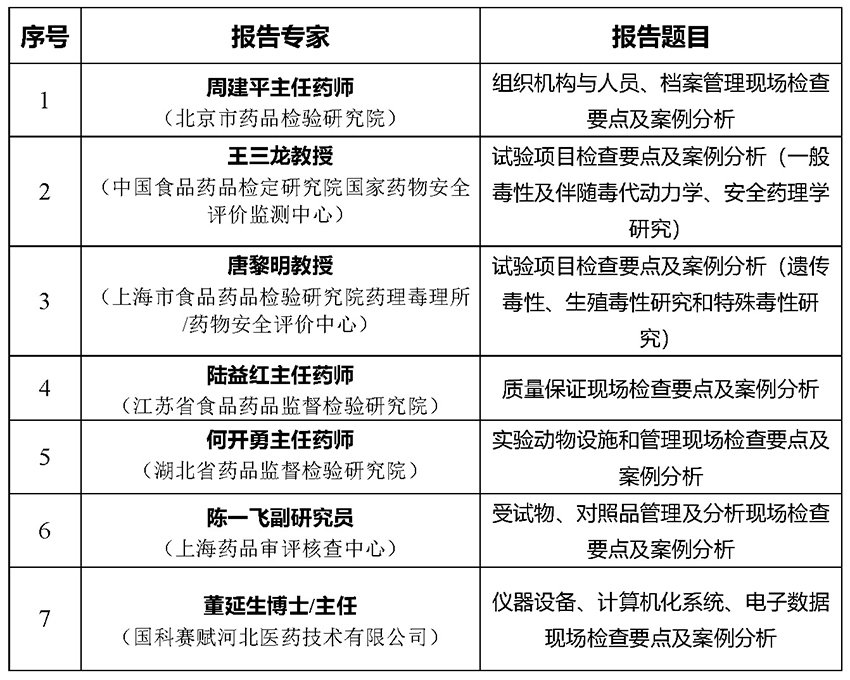
(四)其他分论坛报告)

注:分论坛六邀请国内药物GLP检查专家讲解
五、会议费用
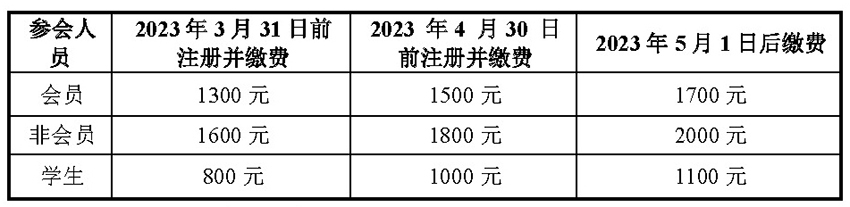
会议费用:(统一安排参会代表食宿,费用自理)
缴费方式(银行汇款):
开户名:中国毒理学会;
开户银行:中国工商银行北京市分行永定路支行;
账号:0200004909014450531。
汇款时请注明:“姓名+广东粤港澳”的字样
发票信息收集二维码:

备注:1.发票内容为:会展服务*会议注册费;2.发票统一开具电子普通发票。
温馨提示:
-
会员是指中国毒理学会会员,广州市生物产业联盟会员及会员单位和广东食品药品审评认证协会会员及会员单位;学生代表请携带学生证;
-
已经于2021年交过注册费用的单位及个人,本次将不再收取,届时直接报到。由于时间间隔较长,请已缴费计划参会人员重新发送报名回执及缴费凭证至指定会务邮箱ywdldh_yga@163.com,以便确认参加本次会议人员实际信息。
-
为了提高工作效率,此次会议全部使用电子发票。凡已开据会议发票的,将不能办理退费手续。
六、参会对象
-
国家和省市食品药品监督管理局药审中心药物毒理审评人员和监管人员;
-
国内各省市药品检验检定所、制药企业(公司)与新药以及医疗器械研发人员;
-
国内外药物安全评价中心、化学物安全评价中心、农药安评中心和医疗器械安评中心的研发与技术人员;
-
医药科研院(所)、药检单位和医药高等院校中从事药物研究的相关人员;
-
香港、澳门和台湾地区创新药物、医疗器械和新化学品监管部门,检测和评价机构负责人、研究和技术人员等;
-
非临床安全评价研究机构的负责人、专题负责人、实验人员等。
七、会议赞助
诚挚欢迎企事业单位赞助本次会议。
八、联系方式
1.报名注册方式(发送邮件回执或二维码进行报名):
1)参加本次会议的代表,可将回执发电子邮件至下列联系人:
蔡洁莹,电话:13113115412,邮箱:caijy@pregene.com;
赖绮雯,电话:13423699765;邮箱ywdldh_yga@163.com;
2)扫描二维码报名

2.论文投稿联系人:
投稿的参会代表,可将稿件发电子邮件至下列联系人:
李淑霞,电话:13726813304;邮箱:csps2019@163.com;
赖绮雯,电话:13423699765;邮箱:ywdldh_yga@163.com。
3. 企业参会代表(药品医疗器械企业推广和产品推广)报名:
王全军,中国毒理学会副秘书长,中国毒理学会药物毒理与安全性评价专业委员会常务副主任委员兼秘书长,中科苏州药物研究院副院长,赛赋医药集团首席科学家,国家北京药物安全评价研究中心,电话:18611782967;邮箱:wangquanjunbeijing@163.com。
杨 威,中国毒理学会副秘书长,中国毒理学会药物毒理与安全性评价专业委员会副主任委员兼秘书长,广东省食品药品审评认证协会GLP与药理毒理专委会主任委员,广州市生物产业联盟副理事长,广东省药物非临床评价研究重点实验室主任,广东省创新药物评价与研究工程技术中心主任,广东莱恩医药研究院有限公司董事长;电话:18928860179,13544561087;邮箱:yangwei0719@163.com。
4. 会议报名及会务总协调人
王全军,电话:18611782967;邮箱:wangquanjunbeijing@163.com;
杨 威,电话:18928860179,13544561087;邮箱:yangwei0719@163.com;
张继帅,电话:13661255174;邮箱:zhangjs@pregene.com。
主办单位:中国毒理学会药物毒理与安全性评价专业委员会
联合主办:广东省食品药品审评认证协会GLP与药理毒理专委会
广州市生物产业联盟
指导单位:深圳市坪山区人民政府
支持单位:深圳市坪山区科技创新局
承办单位:深圳普瑞金生物药业股份有限公司
广东莱恩医药研究院有限公司
国家北京药物安全评价研究中心
广东省药物非临床评价研究重点实验室
国科赛赋(深圳)新药研发科技有限公司
广东省细胞与基因治疗创新药物工程技术研究中心
广东省创新药物评价与研究工程技术中心
国科赛赋河北医药技术有限公司
广州湾区生物医药研究院
协办单位:深圳兴湾生物医药发展顾问有限公司
附1:回执:

附2:酒店信息及交通情况:
一、酒店信息:
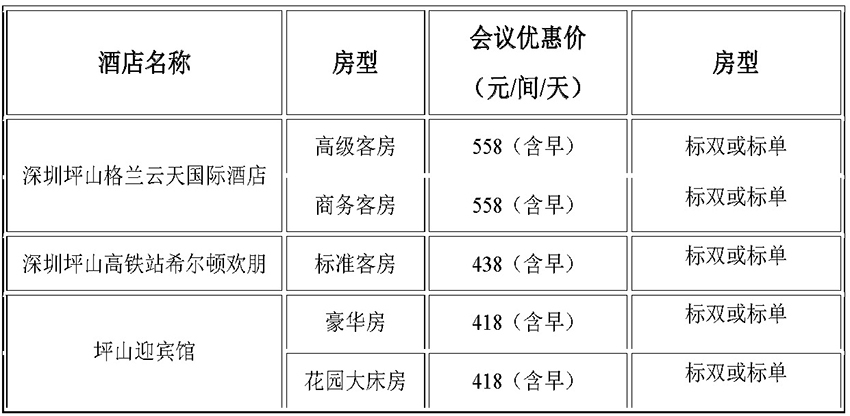
温馨提醒:
1. 由于会议规模较大,会议酒店房间有限,会务组已联系好会场附近的酒店,距离会场较近;
2. 所有参会者先到会议酒店报到。
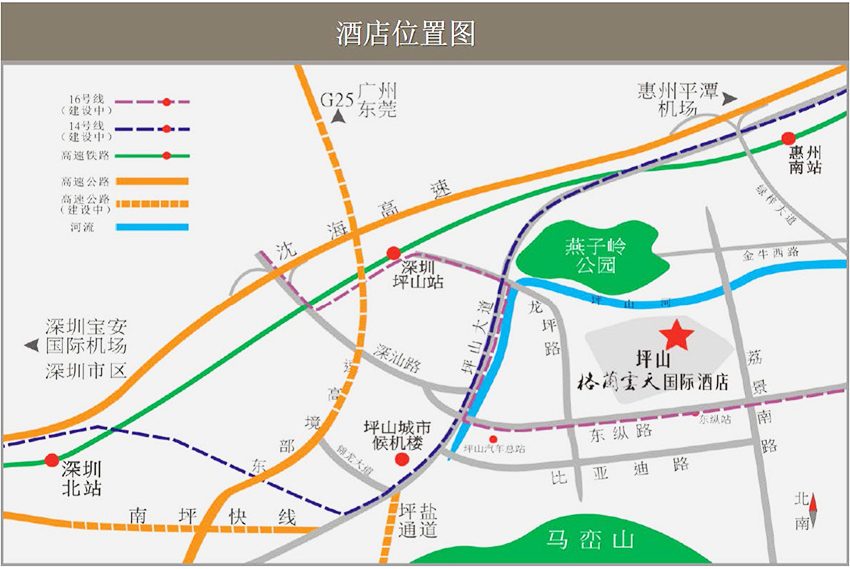
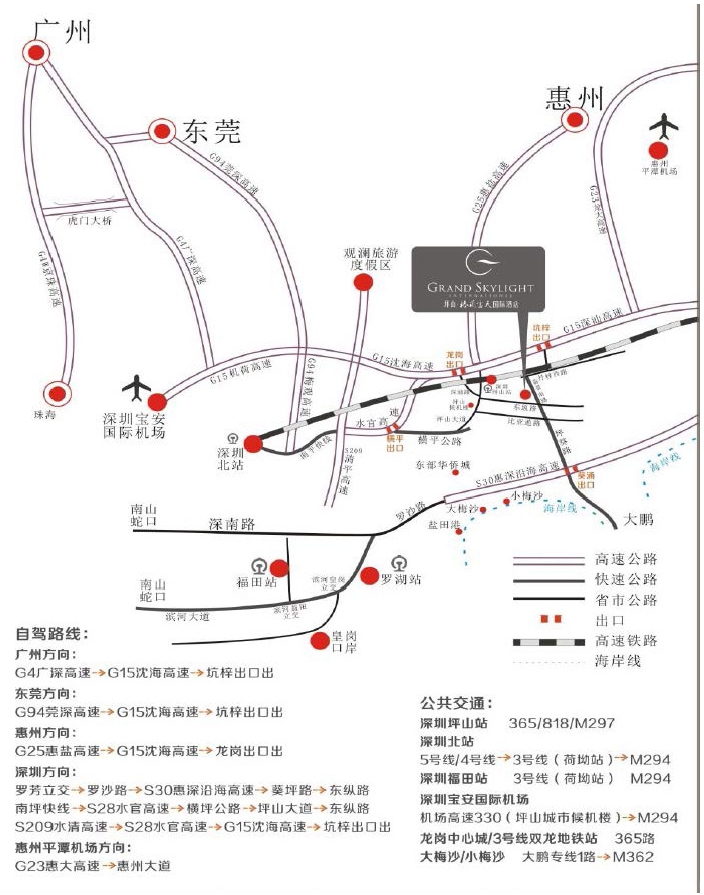
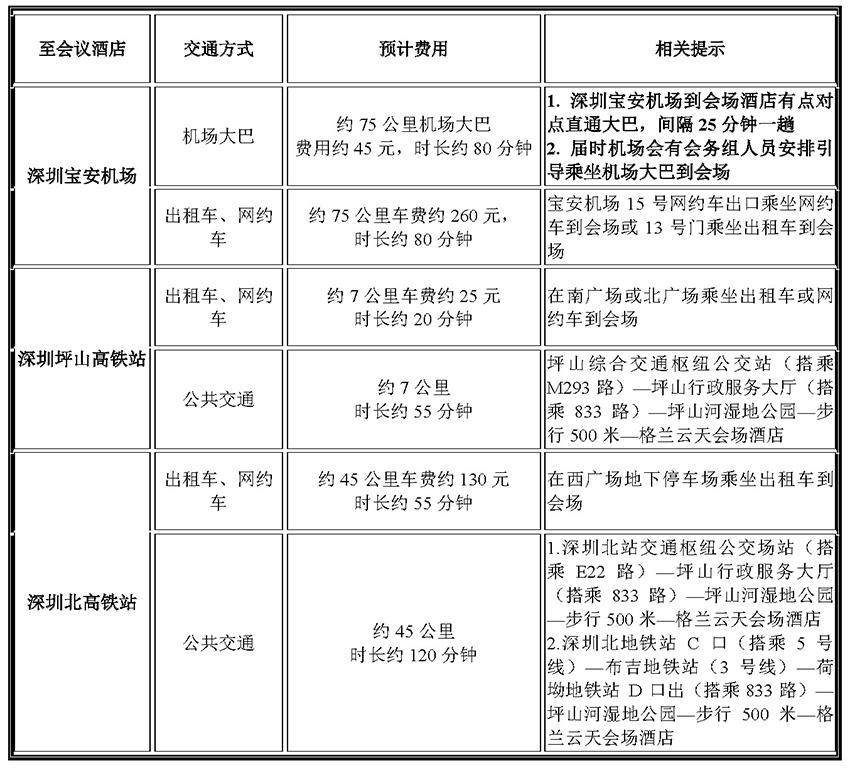
二、交通信息
1. 酒店位置图